Anti-aging through diet
食によるアンチエイジング
アンチエイジングは、単に老化予防というよりも、健康を守ること全般を意味する用語として広く認知されています。当研究室では、そのアンチエイジングを食により実践することを目的に、年齢とともに避けられない「健康の衰え」と、それを防ぐための「食の機能性」に関する研究を行っています。健康の衰えに関しては、最近注目されている異常修飾物(サビのようなもの)の生成とその役割に関する基礎研究を行っています。
一方、食によるアンチエイジングについては、ヒトが生来もつ生体防御機能である解毒と自然免疫に着目し、その防御機能を亢進する食品成分の探索と分子機構解析を進めています。さらに、新たな研究として、核酸や核酸関連タンパク質のアンチエイジング機能探索研究を開始しました。このアンチエイジング研究の魅力を広く伝えながら、新しい独自の分野を開拓したいと考えています。
About Us
1512年春、スペインの探検家フアン・ポンセ・デ・レオンは、“あるもの”を探しにカリブ海に向かいました。その探し物は、“若返りの水”。あらゆるものを得て、最後に手に入れたいものはやはり永遠の命。あるはずのないものを求めて、島から島を巡りましたが、結局断念することになります。
このスペインの探検家のように、いつまでも若く元気でいたいという気持ちは、今も昔も変わらない万人の願いです。しかし、残念ながら老いは避けられません。ある人は容貌の変化から実感するのかもしれませんし、疲労、運動能力の減退、または視覚や聴覚などの感覚機能の変化などで自覚する人もいるでしょう。多くの人は、こうした変化を実感することにより自分の老いを感じるようになります。また、健康の衰えはがんなどの病気への不安を掻き立てるでしょう。
一方、老いは避けられませんが、健康を守る努力をすることはできるでしょう。そして、健康を守るには、運動とともに食が大切であることは誰しも理解しています。先端アンチエイジング研究社会連携講座は、令和7年4月にフォーデイズ株式会社からの支援を受け、研究活動を開始しました。アンチエイジング研究には様々な切り口がありますが、 「健康の衰え」と「食の機能性」の両面からアプローチすることにより、フアン・ポンセ・デ・レオンが求めた“若返りの水”に代わる“健康を守る食”を開発する夢を追いかけたいと思っています。

(引用 Finkel, T. Nature 425, 132-133 (2003))
Research
サビの生成
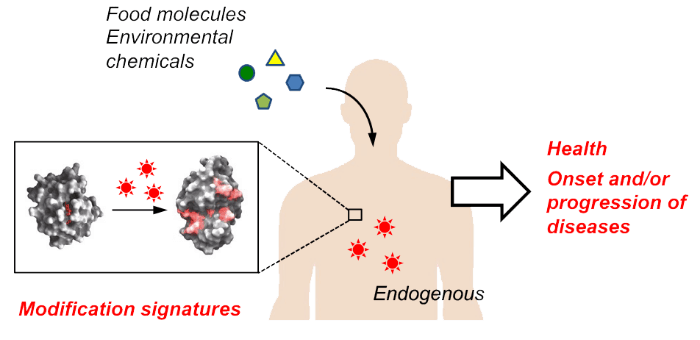
1日あたり6万回。これは一つの細胞の遺伝子が受ける損傷の回数とされています。このような損傷は様々な要因によって起きうるものであり、生涯避けることができない現象です。こうした現象の要因の一つに、生体成分の自然修飾があげられます。
例えば、酸素とブドウ糖という生存に必要不可欠な分子は、自然修飾をもたらす重要な因子です。酸素はもともとビラジカルという活性化されやすい状態にある分子で、様々な酸素活性種の起源であるとともに、脂肪酸の過酸化におけるフリーラジカル連鎖反応でも重要な役割を果たします。また、ブドウ糖を含む還元糖はそのアルデヒド性のためタンパク質などの生体成分と反応性を示します。
このように、人類は効率的なエネルギー産生のために酸素やブドウ糖を必要とし、その代償として、生体成分の自然修飾を受け入れなければなりません。それはすなわち、健康機能の衰え(エイジング)からは逃れられないことを意味します。現在の興味は、自然修飾タンパク質の構造と機能です。エイジングに関連した異常修飾物の実態を知ることは、アンチエイジング研究に不可欠なのです。
自然治癒力:解毒と自然免疫
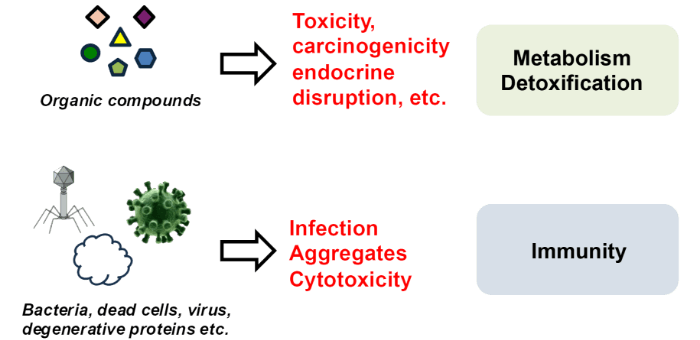
食には3つの機能(一次〜三次機能)があると言われています。生命維持や身体活動に不可欠な一次機能、味覚、嗅覚、美味しさなどの感覚機能である二次機能、そして体調調節や生体防御など健康維持に関連した三次機能です。アンチエイジングはその三次機能のカテゴリーに入ります。健康や病気との関わりから、社会的に注目されているにもかかわらず、その中身がよくわかっていない機能でもあります。
また、三次機能に関連した食品成分は応用(製品化)が優先されがちで、その本質的な機能や分子メカニズムの解明がおろそかになっているものが多いのも否めません。当研究室では、ポリフェノールや含硫化合物など、本来は植物にとって創傷治癒や生体防御などに働いている代謝物のアンチエイジング機能に興味を持っています。特に、生まれながらにして備わっている解毒や免疫などの「生体防御機能」に食品成分がどう働くのか、と言った視点に基づいた研究を推進しています。
核酸および
核酸関連タンパク質の機能性

核酸は遺伝情報としてのDNAとそれを取り巻くタンパク質からなる分子ですが、食として摂取した場合、どのような機能を持つのでしょうか。当研究室では、これまでの「食と自然免疫」に関する研究実績を基盤に、核酸及び核酸関連タンパク質が何らかのアンチエイジング機能を持つのではないか、と言う作業仮説を立て、新たな研究を開始しました。
Publication
- Original Papers
-
-
Yamaguchi, K., Hu, Y. Y., Kawajiri, K., Itakura, M., Nakashima, F., Shibata, T., Uchida, K. (2025) Adductome-based identification of lysine mono-methylation as a key post-translational protein modification in autoimmune diseases. J. Biol. Chem. 110684.
-
Saimoto, Y., Kusakabe, D., Morimoto, K., Matsuoka, Y., Kozakura, E., Kato, N., Tsunematsu, K., Umen,o T., Kiyotani, T., Matsumoto, S., Tsuji, M., Hirayama, T., Nagasawa, H., Uchida, K., Karasawa, S., Jutanom, M., Yamada, KI (2025) Lysosomal lipid peroxidation contributes to ferroptosis induction via lysosomal membrane permeabilization. Nat. Commun. 16(1), 3554-3554.
-
Itakura, M., Yamaguchi, K., Uchida, K. (2025) Moonlight function of antioxidants. Biosci. Biotech. Biochem. 89(2), 187-192.
-
Morimoto, A., Takasugi, N., Pan, Y., Kubota, S., Dohmae, N., Abiko, Y., Uchida, K., Kumagai, Y., and Uehara, T. (2024) Methyl vinyl ketone and its analogs covalently modify PI3K and alter physiological functions by inhibiting PI3K signaling. J. Biol. Chem. 300,105679.
-
Anan, Y., Itakura, M., Shimoda, T., Yamaguchi, K., Lu, P., Nagata, K., Dong, J., Ueda, H., and Uchida, K. (2024) Molecular and structural basis of anti-DNA antibody specificity for pyrrolated proteins. Commun. Biol. 7, 149.
-
Qiu, B., Zandkarimi, F., Saqi, A., Castagna, C., Uchida, K., Toyokuni, S., Miorin, L., Hibshoosh, H., and Stockwell, B. R. (2024) Fatal COVID-19 pulmonary disease involves ferroptosis. Nat. Commun. 15, 3816.
-
Sei, H., Hirade, N., Kamiya, K., Nakashima, F., Yoshitake, J., Kano, K., Mishiro-Sato, E., Kikuchi, R., Uchida, K., Shibata, T. (2024) Isocitrate dehydrogenase 1 upregulation in urinary extracellular vesicles from proximal tubules of type 2 diabetic rats. FASEB J.38(10): e23688.
-
Sasayama, Y., Mamiya, T., Qi, J., Shibata, T., Uchida, K., Nabeshima, T., and Ojika, M. (2023) Neuritogenic steroid glycosides from crown-of-thorns starfish: possible involvement of p38 mitogen-activated protein kinase and attenuation of cognitive impairment in senescence-accelerated mice (SAMP8) by peripheral administration. Bioorg. Med. Chem. 78, 117144.
-
Hirayama, A., Hayasaka, R., Tabata, S., Hasebe, M., Ikeda, S., Hikita, T., Oneyama, C., Yoshitake, J., Onoshima, D., Takahashi, K., Shibata, T., Uchida, K., Baba, Y., Soga, T., and Tomita, T. (2023) Metabolomics of small extracellular vesicles derived from isocitrate dehydrogenase 1-mutant HCT116 cells collected by semi-automated size exclusion chromatography. Front. Mol. Biosci., section Molecular Diagnostics and Therapeutics. 9:1049402.
-
Nakahara, K., Okuda, K., Ito, A., Kumar, A., Nomura, R., Iijima, Y., Takasugi, KN., Adachi, K., Shimada, Y., Fujio, S., Onuma, K., Osaki, M., Okada, F., Ukegawa, T., Takeuchi, Y., Yasui, N., Yamashita, A., Marusawa, H., Katagiri, T., Shibata, T., Uchida, K., Nakamura, T., Zhang, K. Y. J., Lipton, S. A., and Uehara, T. (2023) Pivotal role for S-nitrosylation of DNA methyltransferase in epigenetic regulation. Nat. Commun. 14, 621.
-
Yoshitake, J., Shibata, T., Chikazawa, M., and Uchida, K. (2023) Autoxidation of ascorbate mediates lysine N-pyrrolation. Free Radic. Res. 56, 749-759.
-
Nakashima, F., Loh, W. Q., Wakabayashi, M., Shimomura, H., Hattori, H., Kita, M., Inoue, A., Uchida, K., Shibata, T. (2023) Eriodictyol and thymonin act as GPR35 agonists. Biosci. Biotech. Biochem. 87, 1514-1522.
-
Nishiyama, K., Nishimura, A., Shimoda, K., Tanaka, T., Kato, Y., Shibata, T., Tanaka, H., Kurose, H., Azuma, Y. T., Ihara, H., Kumagai, Y., Akaike, T., Eaton, P., Uchida, K., and Nishida, M. (2022) Redox-dependent internalization of purinergic P2Y6 receptor limits colitis progression. Sci. Signal. 15, eabj0644.
-
Lim, S.Y., Yamaguchi, K., Itakura, M., Chikazawa, M., Matsuda, T., and Uchida, K. (2022) Unique B-1 cells specific for both N-pyrrolated proteins and DNA evolve with apolipoprotein E deficiency. J. Biol. Chem. 298, 101582.
-
Itakura, M., Yamaguchi, K., Kitazawa, R., Lim, S. Y., Anan, Y., Yoshitake, J., Shibata, T., Negishi, L., Sugawa, H., Nagai, R., and Uchida, K. (2022) Histone functions as a cell-surface receptor for AGEs. Nat. Commun. 13, 2974.
-
Yoshitake, J., Azami, M., Sei, H., Onoshima, D., Takahashi, K., Hirayama, A., Uchida, K., Baba, Y., and Shibata, T. (2022) Rapid isolation of extracellular vesicles using a hydrophilic porous silica gel-based size-exclusion chromatography column. Anal. Chem. 94, 13676-13681.
-
Yamaguchi, K., Itakura, M., Tsukamoto, M., Lim, S.Y., and Uchida, K. (2022) Natural polyphenols convert proteins into histone-binding ligands. J. Biol. Chem. 298, 102529.
-
Uchida, K. (2022) Conversion of proteins into DNA mimetics by lipid peroxidation. Arch. Biochem. Biophys. 728, 109374.
-
Komae, S., Kasamatsu, S., Uchida, K., and Ihara, H. (2022) Quantitative determination of 2-oxo-Imidazole-containing dipeptides by high-performance liquid chromatography/tandem mass spectrometry. Antioxidants 11, 2401.
-
Hasegawa, K, Kuwata, K., Yoshitake, J., Shimomura, S., Uchida, K., Shibata, T. (2021) Extracellular vesicles derived from inflamed murine colorectal tissue induce fibroblast proliferation via epidermal growth factor receptor. FEBS J. 288, 1906–1917.
-
Endo, R., Uchiyama, K., Lim, S. Y., Itakura, M., Adachi, T., and Uchida, K. (2021) Recognition of acrolein-specific epitopes by B cell receptors triggers an innate immune response. J. Biol. Chem. 296, 100648-100648.
-
Tisma, V. S., Bulimbasic, S., Ljubanovic, D. G., Galesic, K., Vergles, J. M., Mitrovic, J., Uchida, K., Tatzber, F., Zarkovic, N., Jaganjac, M. (2021) The onset of systemic oxidative stress associated with accumulation of lipid peroxidation product acrolein in the skin of patients with small-vessel vasculitis. Mol. Med. 26(8):2344.
-
Yamaguchi, K., Itakura, M., Kitazawa, R., Lim, S. Y., Nagata, K., Shibata, T., Akagawa, M., and Uchida, K. (2021) Oxidative deamination of lysine residues by polyphenols generates an equilibrium of aldehyde and 2-piperidinol products. J. Biol. Chem. 297, 101035.
-
Kakihana, Y., Kasamatsu, S., Yamakage, A., Uchida, K., and Ihara, H. (2021) Distribution and quantitative analysis of homoanserine and its 2-oxo derivative in mouse tissues. Free Radic. Res. 55, 688-697.
-
Tanaka, H., Hosoi, Y., Ishikawa, K., Yoshitake, J., Shibata, T., Uchida, K., Hashizume, H., Mizuno, M., Okazaki, Y., Toyokuni, S., Nakamura, K., Kajiyama, H., Kikkawa, F., and Hori, M. (2021) Low temperature plasma irradiation products of sodium lactate solution that induce cell death on U251SP glioblastoma cells were identified. Sci. Rep. 16, 18488.
-
Katayoshi, T., Kusano, Y., Shibata, T., Uchida, K., and Tsuji-Naito, K. (2021) Low-molecular-weight whey proteins promote collagen production in dermal fibroblasts via the TGF-β receptor/Smad pathway. Biosci. Biotech. Biochem. 85, 2232-2240.
-
Kasamatsu, S., Komae, S., Matsukura, K., Kakihana, Y., Uchida, K., and Ihara, H. (2021) 2-Oxo-imidazole-containing dipeptides play a key role in the antioxidant capacity of imidazole-containing dipeptides. Antioxidants 10, 1434.
-
Erdélyi, K., Ditrói, T., Johansson, H. J., Czikora, A., Balog, N., Silwal-Pandit, L., Ida, T., Olasz, J., Hajdú, D., Mátrai, Z., Csuka, O., Uchida, K., Tóvári, J., Engebraten, O., Akaike, T., Børresen Dale, A. L., Kásler, M., Lehtiö , J., and Nagy, P. (2021) Reprogrammed transsulfuration promotes basal like breast tumor progression via realigning cellular cysteine-persulfidation. Proc. Natl. Acad. Sci. U.S.A. 118, e2100050118.
-
Fujikawa, K., Nakahara, K., Takasugi, N., Nishiya, T., Ito A., Uchida, K., and Uehara, T. (2020) S-Nitrosylation at the active site decreases the ubiquitin-conjugating activity of ubiquitin-conjugating enzyme E2 D1 (UBE2D1), an ERAD-associated protein. Biochem. Biophys. Res. Commun. 524, 910-915.
-
Petkovic, I., Bresgen, N., Gilardoni, E., Regazzoni, L., Uchida, K., Aldini, G., Siems, W., Eckl, P. (2020) In vitro aging of human skin fibroblasts: Age-dependent changes in 4-hydroxynonenal metabolism. Antioxdiants 9, 150.
-
Feng, H., Schorpp, K., Jin, J., Yozwiak, C. E., Hoffstrom, B. G., Decker, A. M., Rajbhandari, P., Stokes, M. E., Bender, H. G., Csuka, J. M., Upadhyayula, P. S., Canoll, P., Uchida, K., Hadian, K., and Stockwell, B. R. (2020) Transferrin receptor is a specific ferroptosis marker. Cell Rep. 30, 3411-3423.
-
Sasatsuki, H., Nakazaki, A., Uchida, K., and Shibata, T. (2020) Quantitative analysis of oxidized vitamin B1 metabolites generated by hypochlorous acid. Free Radic. Biol. Med. 152, 197-206.
-
Chikazawa, M., Yoshitake, J., Lim, S.-Y., Iwata, S., Negishi, L., Shibata, T., and Uchida, K. (2020) Glycolaldehyde is an endogenous source of lysine N-pyrrolation. J. Biol. Chem. 295, 7697-7709.
-
Luong, N. C., Abiko, Y., Shibata, T., Uchida, K., Warabi, E., Suzuki, M., Noguchi, T., Matsuzawa, A., and Kumagai, Y. (2020) Redox cycling of 9,10-phenanthrenequinone activates epidermal growth factor receptor signaling through S-oxidation of protein tyrosine phosphatase 1B. J. Toxicol. Sci. I45, 349-363.
-
Takamiya, R., Takahashi, M., Maeno, T., Saito, A., Kato, M., Shibata, T., Uchida, K., Ariki, S., Nakano, M. (2020) Acrolein in cigarette smoke attenuates the innate immune responses mediated by surfactant protein D. Biochim. Biophys. Acta 1864, 129699.
-
Ishii, I., Kamata, S., Oyama, T., Saito, K., Honda, A., Yamamoto, Y., Suda, K., Ishikawa, R., Itoh, T., Watanabe, Y., Shibata, T., Uchida, K., and Suematsu, M. (2020) PPARα ligand-binding domain structures with endogenous fatty acids and fibrates. iScience 23, 101727.
CLOSE
-
- Reviews & Books
-
-
中島史恵、柴田貴広、内田浩二 (2024) “食品成分によるタンパク質修飾を介した炎症抑制活性” 日本栄養・食糧学会誌. 77, 125-130.
-
板倉正典、内田浩二 (2022) “タンパク質最終糖化産物 (AGEs)の抗炎症機能” カレントトピックス 実験医学 羊土社 Vol.40, 2637-2640.
-
Niki, E and Uchida, K. (2021) Special issue on “Recent Topics of Redox Chemistry and Biology”. Free Radic. Res. 55, 305-306.
-
Naito, Y., Toyokuni, S., and Uchida, K. (2020) The new era for redox research. Free Radic. Res. 26, 1-7.
内田浩二 (2020) “序に変えて:「医食同源」を解明する食と健康研究の最前線” 実験医学増刊「食と健康を結ぶメディカルサイエンス」 (内田浩二 編集) 羊土社 Vol. 38.
内田浩二 (2020) “リポキシデーションによるタンパク質の自然修飾” 実験医学増刊「食と健康を結ぶメディカルサイエンス」 (内田浩二 編集) 羊土社 Vol. 38, 1605-1609.
中島史恵、柴田貴広、内田浩二 (2020) “システイン残基におけるユニークな自然修飾” 実験医学増刊「食と健康を結ぶメディカルサイエンス」 (内田浩二 編集) 羊土社 Vol. 38, 1622-1628.
CLOSE
-
- Conference Presentations
-
内田 浩二
疾患に関連した翻訳後修飾シグネチャーの構造と機能
第50回日本医用マススペクトル学会年会
2025年9月(一宮)Koji Uchida
Chemoprevention by foods
Redox Chemistry and Biology for Drug Development and Health Management
2025年2月(木甫、韓国)Koji Uchida
Immune memory against toxic aldehydes
The 11th Biennial Meeting of the Society for Free Radical Research-Asia (SFRR-Asia) and the Chinese National Conference of Redox Biology and Medicine 2024
2024年10月(北京、中国)Koji Uchida
Immune memory against toxic aldehydes
HNE club
2024年10月(ジェノバ、イタリア)内田 浩二
毒性アルデヒドに対する免疫記憶(特別講演)
第51回日本毒性学会学術年会
2024年7月(博多)内田 浩二
シンポジウム レドックスシグネチャーの生物学 イントロダクション
第96回日本生化学会大会
2023年11月(博多)内田 浩二
マクロファージによるapoE受容体を介したピロール化タンパク質の取り込み
第96回日本生化学会大会
2023年10月(博多)内田 浩二
シンポジウム 付加体科学とは何か 短寿命活性種に起因する付加体の構造と機能
第96回日本生化学会大会
2023年10月(博多)内田 浩二
付加体発掘40年(特別講演)
日本毒性学会付加体科学部会第1回キックオフシンポジウム
2023年9月(岡山)内田 浩二
シンポジウム 化学物質のアダクト形成を介した新規毒性機構の解明とその検出 酸化に起因した修飾シグネチャーの構造と機能
第50回日本毒性学会学術年会
2023年6月(横浜)内田 浩二
シンポジウム1農学系研究者と医学系研究者からの発信~連携に向けて~、抗酸化剤に起因する修飾シグネチャーの構造と機能
第76回日本酸化ストレス学会学術集会
2023年5月(神戸)内田浩二
2-オキソヒスチジンの発見
第76回日本栄養・食糧学会大会シンポジウム「イミダゾールペプチド研究の新展開」2022年6月(神戸)内田浩二
自然免疫に関与する酸化特異的エピトープ
第64回日本脂質生化学会
2022年6月(東京)内田浩二
タンパク質修飾を介した食の免疫記憶
第49回日本毒性学会学術年会 ワークショップ「エクスポソームの新戦略」
2022年7月(札幌)内田 浩二
酸化ストレス疾患病態解析における分析技術の新展開
第74回日本酸化ストレス学会・第21回日本NO学会合同学術集会
2021年5月(オンライン)内田浩二
抗化剤機能のパラダイムシフト
日本農芸化学会2021年度大会「抗酸化研究の新展開」シンポジウム
2021年3月(オンライン)内田浩二
エキスポソームに備える生体防御系としての自然抗体
第94回日本薬理学会年会「薬理学・毒性学視点からアプローチするエクスポソーム研究」シンポジウム
2021年3月(札幌)内田浩二
リポキシデーションによるタンパク質自然修飾
第73回日本酸化ストレス学会「新しい酸化脂質解析法を用いたオキシリピッドバイオロジー研究」シンポジウム
2020年10月(オンライン)内田浩二
ユニークなタンパク質修飾反応リポキシデーション
第93回 日本生化学会大会「新たな酸化脂質研究の潮流」シンポジウム
2020年9月(オンライン)
CLOSE
Member
Contact
〒113-8657 東京都文京区弥生1-1-1
東京大学
大学院農学生命科学研究科 応用生命化学専攻
先端アンチエイジング研究社会連携講座
東京大学 弥生キャンパス 6号館 4階 401号室
([at]を@に変えて送信してください)